炎症性腸疾患
炎症性腸疾患とは消化管に原因不明の炎症や潰瘍を繰り返し生じ、腹痛や下痢、血便、発熱、体重減少などを主症状とする疾患の総称で、現在は主に潰瘍性大腸炎とクローン病の2つを指します。
潰瘍性大腸炎について
概要
潰瘍性大腸炎は主に大腸の粘膜にびらんや潰瘍を形成し、下痢や粘血便(血液・粘液・膿の混じった軟便)、腹痛、発熱、体重減少、貧血などを主症状とする原因不明の 難治性疾患です。クローン病と同様、寛解と増悪を長期にわたって繰り返し、入院や手術を余儀なくされることもあるため、日常生活に多大なる支障をきたします。
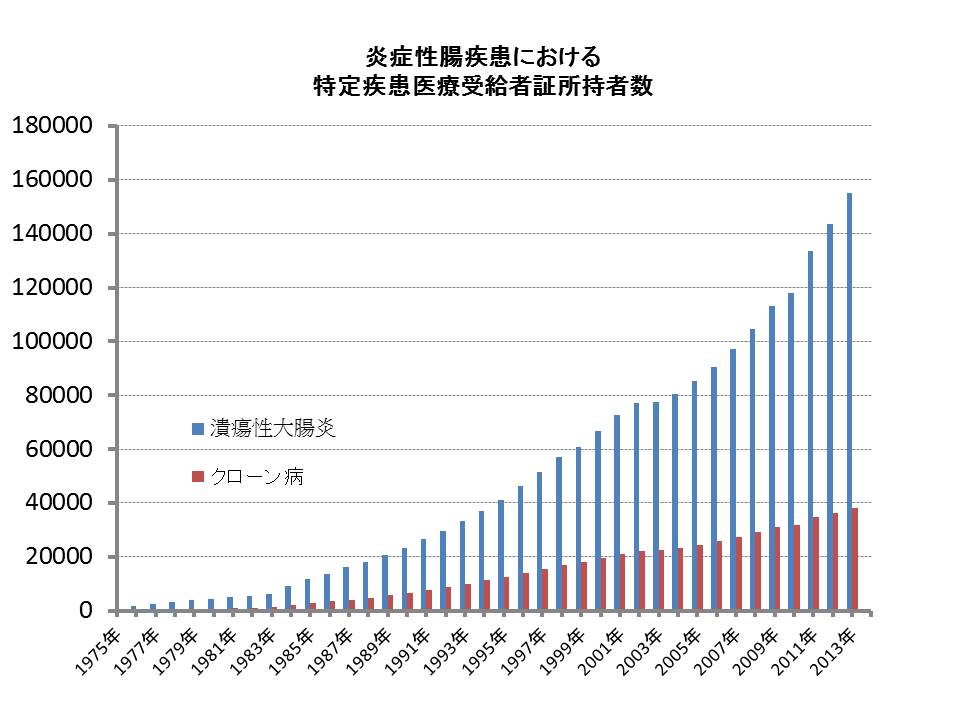
1975年に特定疾患に指定されて以降、特定疾患医療受給者証・交付件数は増加の一途を辿っていて、平成25年度末の患者数(医療受給者証および登録者証交付件数の合計)は 16万6060人。30歳以下の成人に多いですが、小児や50歳以上の年齢層にもみられます。
原因は不明ですが、現時点では遺伝的素因や過剰な免疫反応、消化管バリア機能、腸内細菌叢の異常などが複雑に関与していると考えられています。
病態
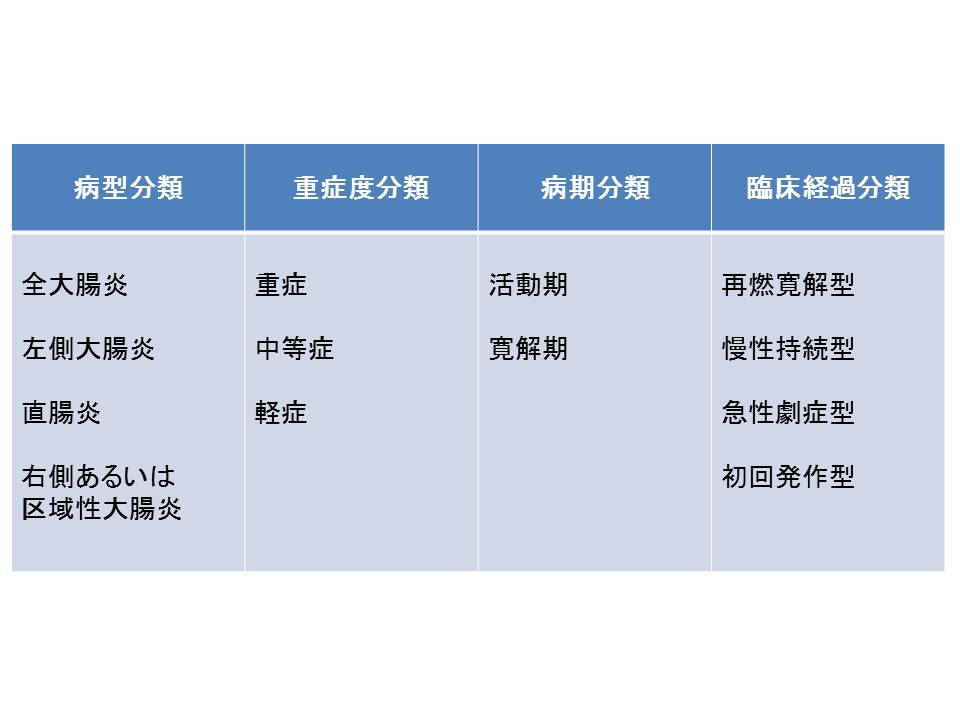
潰瘍性大腸炎の病態は、病変の拡がりや臨床的重症度、臨床経過によって以下のように分類されます。
治療
いまのところ、潰瘍性大腸炎を完治させる治療はありませんが、症状や病情をコントロールしていくことを目的として、大きく内科的治療と外科的治療の2つがあります。
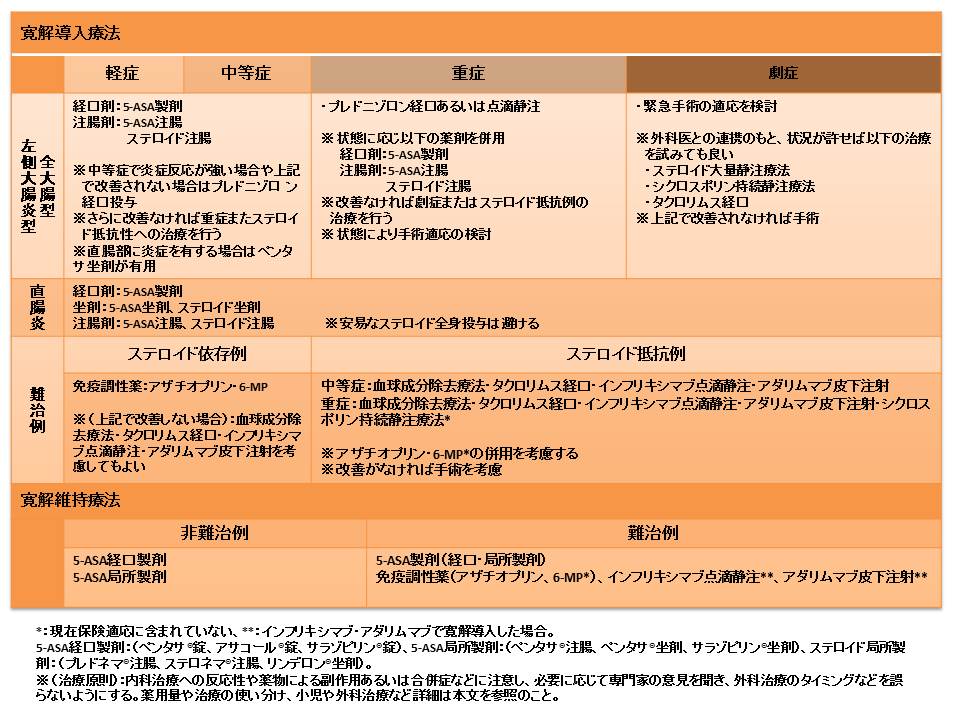
内科的治療では大腸粘膜の異常な炎症を抑え、症状をコントロールすることが目的となります。下に平成25年度潰瘍性大腸炎治療指針(内科)を示します。
潰瘍性大腸炎の基本薬剤は5-アミノサリチル酸(5-ASA)であり、日本で使用可能な5-ASA製剤としてサラゾピリン®、ペンタサ®、アサコール®があります。
サラゾピリン®は腸内細菌でスルファピリジンと5-ASAに分解されて大腸で作用します。
ペンタサ®錠は5-ASAを腸溶性のエチルセルロースの皮膜でコーティングすることで小腸から大腸までの広い範囲で放出されるよう調節されています。
アサコール®錠は回腸末端から5-ASAを放出するpH依存型の放出制御特性を持つコーティングが施されています。このコーティングはpH7以上で崩壊する高分子ポリマーからなり、より下部の消化管(回腸末端から大腸)に到達してから5-ASAが放出されます。
<軽症から中等症の遠位(左側型)潰瘍性大腸炎(直腸炎型を含む)の寛解導入療法 >
①経口5-ASA製剤(サラゾピリン®3~4g/日、ペンタサ®1.5~4g/日、アサコール®2.4~3.6g/日)の内服で治療を行います。直腸炎型の場合、経口投与よりも局所の薬物投与により効果を認めることが多いため、サラゾピリン®坐剤(1~2g/日)、ペンタサ®坐剤(1g/日)、リンデロン坐剤(1~2㎎/日)を使用する場合があります。またペンタサ®注腸もよく使用されます。
②上記内服でコントロール不良の場合はステロイドの注腸および経口投与を考慮します。ただしステロイドの全身投与は安易に行うべきではなく、使用前には有効性だけでなく生じうる副作用についてもきちんと説明をします。特に中心性肥満や満月様顔貌(ムーンフェイス)など容姿に変化をきたす副作用に関しては、思春期の患者が多いため十分納得がいくよう説明がなされるべきです。
<軽症から中等症の全結腸型潰瘍性大腸炎の寛解導入療法>
①まずは5-ASA製剤2g/日以上の投与をおこないます。5-ASA製剤は用量依存性に効果を示すことから、ペンタサ®であれば4g/日、アサコール®であれば3.6g/日の投与が望ましいとされています。
②十分量の5-ASA製剤の投与にも関わらず効果が乏しい場合はプレドニゾロン(PSL)30~40㎎の投与を検討します。近年ではPSL投与前に血球成分除去療法が行われる場合もあります。
③PSLの効果が得られれば、再燃に注意しながらPSLを減量していきます。一般的には1週間に5mg程度の減量が行われます。効果が不十分、あるいは原料に伴い症状の悪化が認められるときには、血球成分除去療法や免疫調性薬の投与を併用し、ステロイドの減量を試みます。長期間のステロイド投与は全身に対する種々の副作用を出現させる可能性が高まり、さらにステロイド自体が上皮再生の遷延をきたすことから、漫然とした投与は避けられるべきです。
<難治例に対する治療法>
潰瘍性大腸炎難治例の定義は、
①ステロイド依存例:PSLの減量に伴って増悪・再燃が生じ、ステロイド離脱困難 。
②ステロイド抵抗例:ステロイドの適正投与にも関わらず1~2週間以内に明らかな改善が得られない場合。
とされています。
重症潰瘍性大腸炎の治療については原則入院治療を考慮すべきであり、経静脈的ステロイド投与が適応となります。静注投与量は1~1.5㎎/㎏/日(40~60㎎/日)とされますが、副作用も多いです。
◎血球成分除去
血中に存在する組織障害の予備軍と考えられている白血球(顆粒球、単球、活性化リンパ球)を特殊な除去器で血中から除去するものです。免疫の悪循環や局所組織障害に関与すると思われる白血球を直接除去し、免疫調性を行う治療法です。日本で開発されたものであり、2種類の方法に大別されます。
①ポリエステル繊維を用いた血球成分除去療法(セルソーバ®E)
白血球が3μm以下の繊維に付着する性質を利用し、旭化成メディカル社が開発した白血球除去器に血液を約50ml/分で通し、顆粒球、単球をほぼ100%、リンパ球を約60%除去します。
②酢酸セルロース製ビーズを用いた白血球除去療法(アダカラム®)
ヘパリンで抗凝固化した全血液をJIMRO社が開発した酢酸セルロースのビーズを充満させた顆粒球除去カラムのなかへ約30ml/分で通し、カラムの前後で約60%の顆粒球と単球を除去します。
血球成分除去療法は基本的には週1回施行し、5~10週間継続します。活動性の高い症例に対しては週2回施行可能です。
◎免疫調性薬
①ステロイド依存の難治症例に免疫調性薬が使用される場合が多いです。主にアザチオプリン(azathioprine:AZA(イムラン®))や、AZAの副作用で投与が継続できない場合はメルカプトプリン(mercaptoprine:6-MP(ロイケリン®)、保険適応外)が使用されることが多いです。血球成分除去療法やタクロリムスを使用することによりステロイド離脱を試みても良いですが、これらを用いた寛解維持治療は認められていません。
②チオプリン製剤の投与量:AZAの初期投与は25~50㎎。投与1週間後に血液生化学検査を実施し、問題なければ投与量を50㎎に増量します。増量2週間後(または以内)に診察し、問題なければ1~2か月ごとに採血を行います。薬剤効果発現までには個人差がありますが2~4週間と考えます。
ただし効果が最大限となるためには2~3か月必要と考えられ、AZA50㎎で効果が認められる場合が多です。悪心、嘔吐など消化器系の副作用が時としてみられますが、この場合は6-MPに変更することで投与が継続可能となる場合が多いです。
チオプリン製剤の副作用としては(ⅰ)投与初期3~4週間以内に生じるアレルギー性のもの。(ⅱ)治療経過途中で見られる用量依存性非アレルギー性のものが挙げられます。症状については白血球減少が最も多いです(2~5%)
AZAによる骨髄抑制は治療経過中にいつでも起こり得ます。膵炎は1.3~3.3%で認められ、投与量に非依存性であり、3~4週間以内に生じるとされています。投与を中止すれば改善します。
発熱、発疹、関節痛などもみられることがありますが投与量とは関係なく、薬物中止で消失します。
◎シクロスポリン
ステロイド治療を7~10日間行っても反応しないステロイド抵抗症例にはシクロスポリンの持続点滴や外科治療を考慮します。シクロスポリンによる効果を期待する場合、比較的高い血中濃度を維持する必要があり、中心静脈栄養下に3~4㎎/㎏のシクロスポリンを24時間持続投与で行います。
多くの場合は1週間程度で臨床症状の改善を認めるとされていて、投与期間については原則2週間以内です。それ以上の投与は高血圧、てんかん発作、感覚異常、振顫、歯肉腫脹、多毛症、電解質異常、日和見感染、腎機能障害など副作用の危険が高まります。
◎タクロリムス
平成21年度の厚生労働省科学研究班における治療指針案には、ステロイド依存・抵抗症例に対する治療法にタクロリムス(プログラフ®)の経口投与が記載されました。タクロリムス製剤には、顆粒、カプセル、注射液がありますが、潰瘍性大腸炎に適応が認められたのはカプセルのみです。タクロリムスは腸管からの吸収に関しては胆汁や粘膜障害の影響を受けることが少ないため、経口のシクロスポリンよりも血中トラフ値の安定性が高いとも言われています。このような点からタクロリムスは潰瘍性大腸炎に対してシクロスポリンとほぼ同等またはそれ以上の効果を示すと考えられています。
血中トラフ値が目標値に達したのち症状が改善傾向にあればステロイドの減量を開始していきます。副作用としては振顫やほてり感、頭痛などの症状が挙げられます。また高濃度では腎機能障害(クレアチニン、K、BUN(血中尿素窒素)の上昇、血糖上昇などが報告されています。
◎生物学的製剤
平成22年度の治療指針案にはインフリキシマブ(レミケード®)の投与もステロイド依存・抵抗性潰瘍性大腸炎の治療薬として記載されています。レミケード?は炎症性サイトカインの1つでTNF-αに対するモノクローナル抗体であり、約2か月間血中に存在するとされています。他の治療法などの適切な治療を行っても、疾患に起因する明らかな臨床症状が残る場合にレミケード®の投与を考慮します。しかしながら寛解維持効果は確認されていないため、寛解導入後は本剤の継続投与の必要性を検討し、他の治療法への切り替えを考慮する必要があります。
平成25年にはアダリムマブ(ヒュミラ®)が既存治療抵抗性の潰瘍性大腸炎の治療薬として認可されました。
抗TNF-α抗体製剤使用にあたっては副作用に結核感染、B型肝炎の再活性化の問題があるため、治療中のモニタリングに注意します。
参考文献
日本医師会雑誌 第114巻・第1号 2015年 日本医師会
クローン病について
概要
クローン病とは口腔から肛門までのあらゆる部位に炎症の再燃と緩解を繰り返す慢性の炎症性疾患です。
1932年にニューヨークのマウントサイナイ病院の内科医、ブリル・バーナード・クローンらによって「限局性回腸炎」として最初に報告され、その後に病名が改められました。
当初の病名のように回腸末端から盲腸にかけての「回盲部」が好発部位です。
クローン病は主に10歳代後半~20歳代の若年者に多く、男女比は2対1で男性に多くみられます。平成25年度の特定疾患医療受給者証交付件数は3万9799人と年々増加しています。
主に小腸と大腸に病変が生じますが、上述の通り特に小腸末端部(回盲部)が好発部位です。非連続性の病変(病変と病変の間に正常部分が存在する)を特徴とし、それにより腹痛や下痢、血便、体重減少などを呈します。
クローン病の原因はいまだはっきりとはわかっていませんが、遺伝的要素や細菌、ウイルスによる感染症、摂食物の何らかの成分に対する腸管粘膜の異常反応、腸管の血流障害などが報告されてきました。また近年、何らかの遺伝的要素を背景とし、腸内の免疫担当細胞が摂食物や腸内細菌に対して過剰に反応することが病気の発症や増悪に関与しているとも考えられています。
主症状は腹痛、下痢、体重減少、発熱、肛門病変などです。まれに虫垂炎との診断で開腹手術の時にクローン病とわかるケースや、腸閉塞、腸穿孔、大量の下血など重篤な症状で判明することもあります。腸管外合併症として、末梢の関節炎や強直性脊椎炎、口腔内アフタ、結節性紅斑、虹彩炎、小児では栄養の吸収不良による成長障害などがみられます。長期経過例においては悪性腫瘍の発症にも注意を必要とします。
クローン病の治療は重篤な合併症などがない限り、基本的に内科的な治療が中心となります。栄養療法と薬物療法があり、重症度や症状の程度などによって方針が分かれ、それにより使用する薬物などが異なってきます。
治療
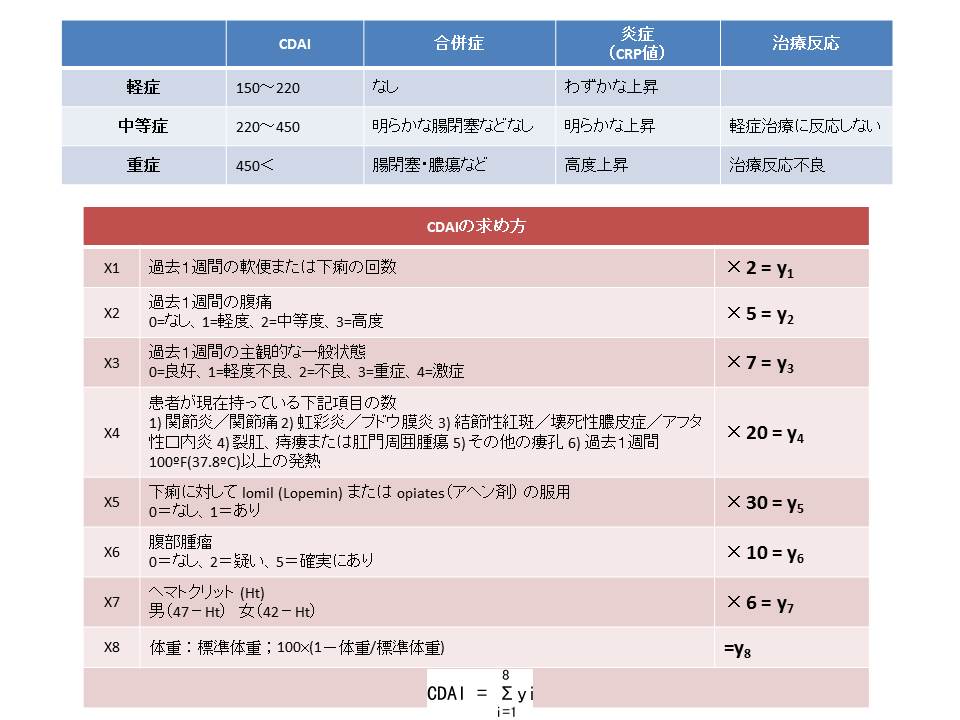
下の図はIBD調査研究班が提唱する本邦のクローン病治療指針案ならびにクローン病重症度分類を示したものです。
軽症では5-ASA製剤が第一選択薬となります。また栄養療法も有用で、両者を併用することもあります。これらで効果不十分の場合には中等症~重症の治療方針に移行します。
中等症~重症では経口ステロイドを投与し、漸減中止します。ステロイドの減量・離脱が困難な時には免疫調整剤であるアザチオプリン(AZA、商品名イムラン)や6メルカプトプリン(6-MP、現在保険適応に含まれていない)の併用も考慮していきます。
我が国では以前から瘻孔を有する患者に6-MPの少量投与(30~50㎎/日)が行われており、約6割のケースで瘻孔の閉鎖、改善が認められています。
ステロイドや栄養療法の寛解導入療法が無効→抗TNF-α抗体製剤(商品名レミケード)の投与を考慮します。
病勢が重篤および高度な合併症を有する重症例では外科治療の適応を検討したうえでステロイドあるいは抗TNF-α抗体製剤の投与を検討します。
著しい栄養低下、頻回の下痢、広範な小腸病変の病勢が重篤な場合、腸管の高度狭窄、瘻孔、膿瘍形成、大量出血、高度の肛門病変などを有する場合や通常の経腸栄養療法が困難な場合は完全静脈栄養療法(TPN)を行います。
瘻孔に対しては外科的治療の適応を検討します。薬物療法としては抗TNF-α抗体製剤が使用されます。AZAも外瘻に有効な場合があります。治療を徐々に強化するステップアップ療法が一般的であるが、難治化の危険因子(若年発症例、穿通性病変や肛門病変の合併、腸管切除を要する、ステロイド投与を要する)を有する場合には抗TNF-α抗体製剤を先行して投与するトップダウン療法により良好な臨床経過が得られる可能性が示唆されています。
寛解維持療法としては在宅経腸栄養療法や薬物療法(5-ASA製剤、AZAなど)が用いられます。AZAは腸管病変のほか肛門病変の寛解維持にも有効です。また抗TNF-α抗体製剤により寛解導入された後は、定期的投与が寛解維持に有効です。在宅経腸栄養療法では1日の摂取カロリーの半分量以上に相当する成分栄養剤の投与が寛解維持に有用です。短腸症候群など在宅経腸栄養療法でも栄養管理が困難な症例では在宅中心静脈栄養法を考慮します。
<栄養療法>
成分栄養剤による経腸栄養療法の寛解導入効果は活動期においてステロイドと同等とされ、腸管病変の改善に優れています。また30kcal/㎏/日以上の成分栄養の継続が再燃防止に有効であることも示されていて、小腸病変に対してより効果的です。TPNは活動期の著しい栄養低下、頻回の下痢、広範な小腸病変の病勢が重篤な場合、腸管の強度狭窄、瘻孔、膿瘍形成、大量出血、高度の肛門病変などを有する場合に適応となりますが、個々の病状に応じて栄養法を選択する必要があります。またTPNは経腸栄養療法と同等の寛解導入効果を有することが明らかにされており、病状が安定すれば経腸栄養療法に移行します。
経腸栄養療法は成分栄養剤(エレンタールR)を経鼻もしくは経口投与します。当初は低濃度少量から開始し、注意しながら投与量と濃度を漸増して数日かけて維持量に移行していきます。1日の維持投与量として理想体重あたり30kcal以上を目標として投与。成分栄養剤を用いる場合には10~20%脂肪乳剤200~500mLを週1~2回点滴静注。また亜鉛や銅などの微量元素欠乏にも注意します。
<薬物療法>
◎5-ASA製剤(サラゾスルファピリジン、メサラジン)
軽症~中等症のクローン病に対してまず5-ASA製剤から開始します。サラゾスルファピリジンは5-ASAとスルファピリジンの結合体であり、主に大腸で効果を発揮します。これに対してメサラジンは5-ASAの徐放性製剤で、小腸上部から抗炎症作用を発揮します。しかし基本的にクローン病に対して寛解維持効果はないと考えられています。
◎ステロイド
中等症~重症の症例や、軽症でも5-ASA製剤に反応しない活動期症例が適応となります。経口ステロイド(プレドニゾロン40㎎/日程度)を投与します。寛解導入効果に優れるが寛解維持効果はないとされています。易感染性、満月様顔貌、骨粗しょう症、耐糖能異常等の副作用を回避するために長期使用は避けられています。
◎血球成分除去療法
ステロイドや栄養療法に対して難治性・抵抗性の急性期患者やインフリキシマブ投与困難例・効果減弱例に対して、リンパ球・単球・顆粒球除去療法が適応となりました。潰瘍性大腸炎と同様のスケジュールで使用します。
◎免疫調整薬
チオプリン製剤であるAZAと6-MP(保険適応外)はCDの寛解導入には有効ですが、効果発現までに数週間~3か月程度を要します。一方、安定した寛解維持効果を有し、またステロイド減量効果もあるためステロイドからの離脱にも有用です。いずれの薬剤も体内で種々の酵素代謝を受け、チオグアニンとなり免疫抑制作用を発揮します。
AZAは有効である限り3~4年は継続することが望ましいとされますが、明確な投与期間設定はありません。副作用は、投与初期に投与量とは無関係に出現する発熱、発疹、悪心、下痢、膵炎や、投与量や代謝に依存する骨髄抑制、脱毛、感染、肝障害などです。少量から投与を開始し、頻回に血液データを確認することが重要です。
◎抗菌薬(保険適応外)
海外ではメトロニダゾールやシプロフロキサシンなどの抗菌薬の長期投与がCDの大腸病変や肛門病変に有効性を示すとの報告があります。
◎抗TNF-α抗体製剤
本邦では現在インフリキシマブとアダリムマブが保険適応になっています。前者はマウスタンパクを含むキメラ型抗体製剤で、後者は完全ヒト型抗体です。いずれもCDの炎症持続に関するTNF-αの中和作用を有し、さらにインフリキシマブは抗体依存性細胞死の誘導に強力な抗炎症作用を発揮。寛解導入・維持療法として有効であり、瘻孔閉鎖維持効果も有します。
一方で重症感染症や日和見感染症のリスク上昇、潜在性結核菌感染症の顕在化の報告があります。近年ではB型肝炎ウイルスの再活性化の可能性も指摘されています。また、抗体製剤に特有の副作用として、投与時反応や遅延型過敏反応による全身反応、製剤に対する抗体産生による効果減弱(二次無効)もあります。
インフリキシマブは寛解導入療法として5㎎/㎏を0,2,6週に投与します。この治療で50~60%の高い緩解導入率を有します。以降は同量を8週間隔で維持投与します。効果減弱が認められた場合は10㎎/㎏への増量が可能です。
アダリムマブは初回160㎎皮下投与、2週間後に80㎎、さらに2週間後から40㎎隔週の維持投与に移行します。寛解導入効果は40~50%です。
◎内視鏡的バルーン拡張術
従来よりCDの大腸狭窄に対して内視鏡的バルーン拡張術が施行されてきましたが、近年では小腸狭窄に対しても可能となりました。CDにおけるバルーン拡張術は腸閉塞症状を伴い、比較的短く屈曲が少ない両性狭窄で、深い潰瘍や瘻孔を伴わないものが良い適応とされています。内視鏡観察下に造影を行い、狭窄部の性状と狭窄長を確認後にバルーンで拡張します。偶発症である穿孔と出血に注意し、慎重に施行すれば再狭窄に対しても反復して施行が可能で、手術回避効果も得られます。
参考文献
日本医師会雑誌 第114巻・第1号 2015年 日本医師会
炎症性腸疾患に対する鍼灸治療の考え方
開業鍼灸師という立場で炎症性腸疾患に対応する場合、主に寛解期から入院を必要としない活動期の軽症、および軽症寄りの中等症までを鍼灸治療の対応可能範囲と考えます。腹痛や下痢がひどく体重の減少が著しい場合や栄養状態の維持が難しく悪化の一途を辿るようなときには鍼灸治療だけで対応するのは困難であり、入院を勧め適切な治療を受けられるよう配慮すべきです。鍼灸だけでなんとかしようして医療機関への適切な受診機会を逃してしまえば、軽症で済むものが重症化してしまう可能性もありますので、施術者も患者さんもこのことは常に意識しておくべきです。
炎症性腸疾患の鍼灸治療は大きく寛解期と活動期の2つに分けられます。
寛解期には暴飲暴食や刺激物の大量摂取など、いわば無茶な食生活をしない限り、クローン病においては低脂質・低残渣の食事を意識しつつもいろいろな食材や料理に挑戦して自分の身体に合うものを探していきましょう。また、食事とエレンタールを組み合わせて体重を増やし、体力の向上・維持を図ります。
散歩やストレッチ、体操、ヨガ、太極拳などの比較的軽度な運動を取り入れ、負担のない範囲で体を動かすようにしましょう。腹部の血流を良くし、またストレス解消やストレスに対する抵抗力をつける体づくりにも繋がります。
夜はできるだけ早く就寝するようにします。例えば睡眠を6時間取るとした場合、22時に寝て4時に起きるのと1時に寝て7時に起きるのとでは、前者の方が睡眠の質が遥かに良好で、日中も眠くなりにくく仕事の効率がアップします。
鍼灸治療は「胃腸力」、すなわち消化吸収力の強化を中心に行います。せっかく食べた物も、消化吸収されなければ身にならず体力の向上も図れません。漢方的には「健脾」(脾を健やかにする)という考え方で治療にあたります。ここでいう「脾」とは現代医学の「脾臓」のことではなく、胃腸を中心とした消化器の働きのことを意味します。
もちろん寛解期で症状が落ちついていても、定期的に血液検査や内視鏡検査などをうけていただくことは必須です。症状が落ち着いていても炎症反応が高値を示したり、内視鏡的に病気が進行していることもあるので、それに応じて使用するツボや道具なども変更していきます。
一方、活動期(軽症~軽度中等症)においてはまず「休腸」、すなわち腸を休めることが必須です。在宅では炎症が落ち着くまでできる限り消化が良く腸に負担のかからないものを摂りつつ、経腸栄養剤でカロリーを確保しながら内服薬を使用する形になってきます。可能であれば絶食して経腸栄養剤のみでカロリーを確保し腸を休めるほうがより有利でしょう。
ドイツで発表された研究によると、軽症から中等症のクローン病の患者(2004年)および潰瘍性大腸炎の患者(2006年)に対する鍼灸治療において、10回の治療(4週間~5週間)後に疾患活動指数やQOLの改善効果が示されました。さらに2014年に中国で発表された研究では、同じく軽症から中等症のクローン病患者に対する鍼灸治療で、週3回、12週間の治療後に活動指数やQOL、血液学的所見(炎症反応、ヘモグロビン)、病理組織スコアの改善効果が認められました。
腹痛や下痢などの症状が落ち着き、各種検査で寛解導入が確認されてきたら1~2週間に1回の治療を継続し、症状が再燃してきたら1週間に2回程治療を集中していくことで寛解導入を早め、寛解維持を図ります。
病院での治療に鍼灸治療を併用することの主なメリットは以下の通りです。
①上述の通り、鍼灸治療は消化器系の働きを高め、食べた飲食物が体の中で活用される形にするのを助ける働きがあります。これにより体力をつけ、免疫系の働きを正常化し、炎症性腸疾患が再び暴れにくくする体質作りをしていきます。
②病院の治療で使用する薬は、ただ体の中に入るだけではその働きを発揮することはできません。体の中に入ったのち、それがきちんと吸収され、かつ病変部位まで到達することが必要不可欠です。
ところが体力が充実していなかったり、あるいは血流が悪い状態だと、体内に取り入れた薬が十分に吸収されなかったり、病変部位まで届きにくくなって、本来の薬効を十分に発揮できなくなってしまいます。
同じ病気で同じ薬を使っているのに効果が現れる人とそうでない人がいるのは、体力の有無や血流の良し悪しなど患者さんごとに体質が異なるためです。
鍼灸や漢方など東洋医学の得意とするところはまさに体質改善です。体質を改善し、体力や血流をアップすることで西洋薬が効きやすくするようバックアップできるのも、西洋医学に東洋医学を併用するメリットの1つです。
参考文献
全日本鍼灸学会雑誌 第65巻別冊(抄録号)
第64回公益社団法人 全日本鍼灸学会学術大会 ふくしま大会抄録集